GAMMAGRAFÍA DE TIROIDES
Dr. Hans Bowles
1. RADIOFÁRMACO
- Solución de pertecnetato [99mTc] de sodio
- Transporte activo del ión 99mTcO4 a través de la membrana basal de las células tiroideas, sin presentar organificación. Se concentra en la glándula tiroides, glándulas salivares, plexo coroideo y mucosa gástrica.
- Transporte activo del ión a través de la membrana basal de las células tiroideas. El yoduro es oxidad para incorporarse a los residuos tirosilo de la tiroglobulina.
2. INDICACIONES
- Valorar estado funcional del tiroides / nódulo(s).
- Seleccionar nódulo a biopsiar.
- Clasificación y estudio del hipertiroidismo.
- Localización de tiroides ectópico.
- Tipificar el posible origen tiroideo de una masa extratiroidea.
3. CONTRAINDICACIONES
- Relativa: embarazo.
- Precaución en caso de lactancia.
4. PROTOCOLO
4.1 Preparación del paciente:
- Posponer la gammagrafía si administración previa de compuestos yodados.
- Contrastes yodados: posponerla al menos 3 meses.
- Amiodarona: puede influir en la captación del 99mTc o del 1231 durante 2 años.
- Tener en cuenta otras posibles fuentes exógenas de yodo: hormonas tiroideas, algunos antitusígenos, algunas cremas anticelulíticas, antisépticos tópicos (povidona yodada), suplementos alimentarios o dietas ricas en yodo.
- Algunos otros fármacos también pueden interferir en la captación del 99mTc (corticoides, interferón, etc.).
- Los antitiroideos de síntesis no alteran el atrapamiento del 99mTc. Sí que disminuyen la organificación del yodo (formación de hormonas).
5. BIBLIOTECA DE IMÁGENES
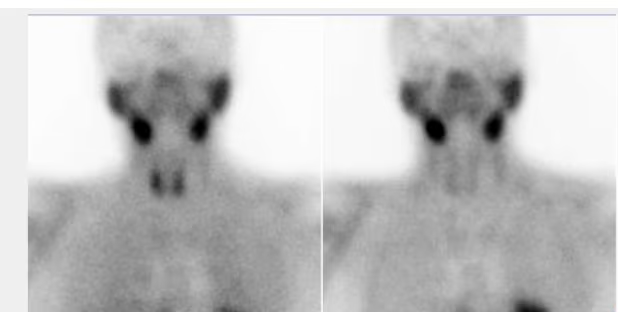
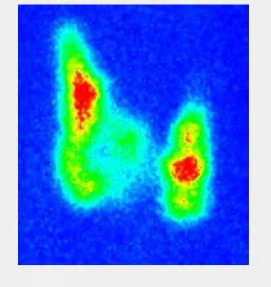
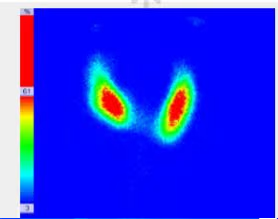
- Fig. 1: Gammagrafía tiroidea normal. Distribución de la actividad simétrica y homogénea (180 kcts en 420 seg)
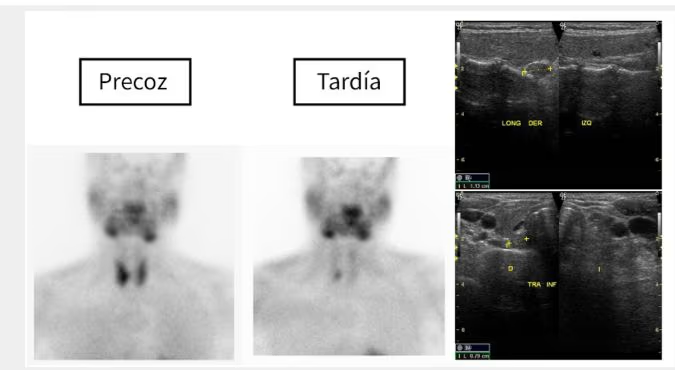
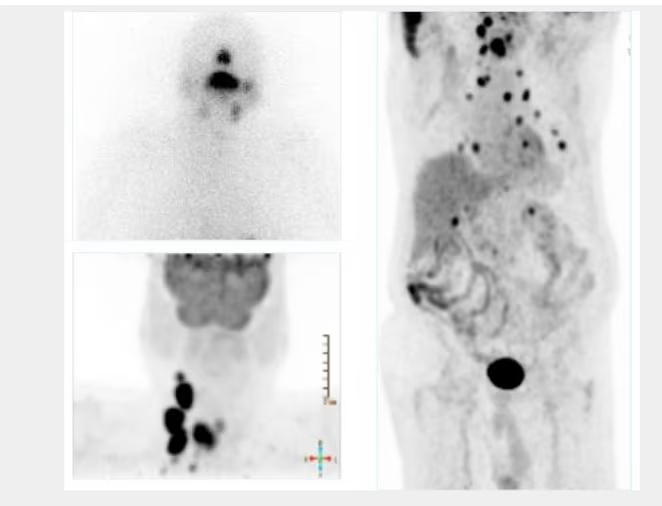
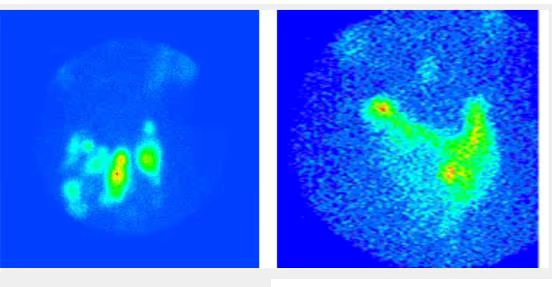
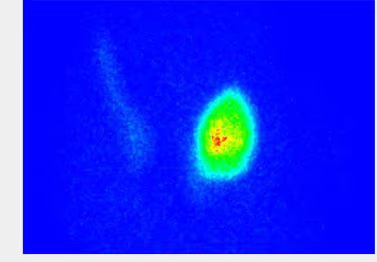
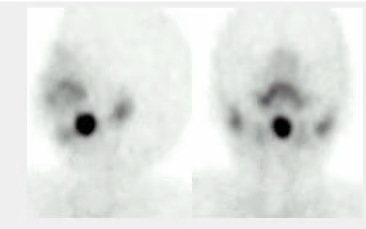
- Fig. 2: Nódulo funcionante izquierdo e hipofuncionante derecho de mayor tamaño, subsidiario de PAAF
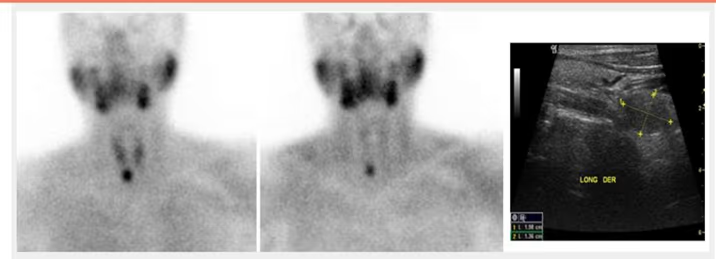
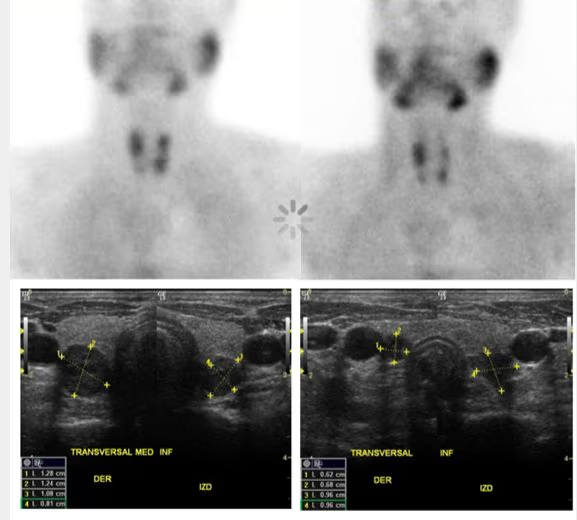
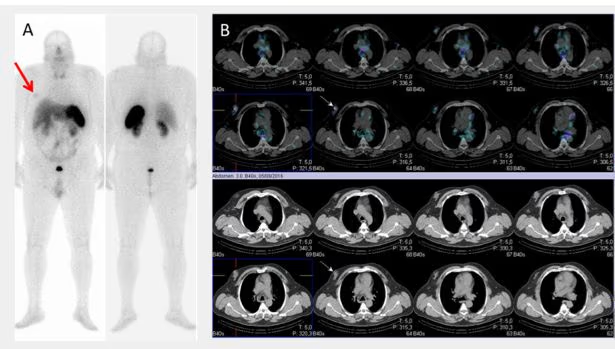
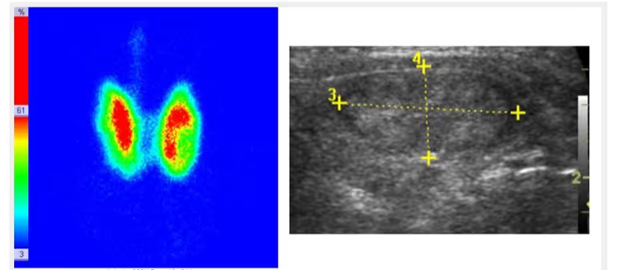
- Fig. 3: Izquierda: BMN mixto (con nódulos hiper e hipocaptantes) con un nódulo hipocaptante de gran tamaño en el lóbulo derecho, a seleccionar para la PAAF. Derecha: BMN con nódulo frío dominante en lóbulo derecho.
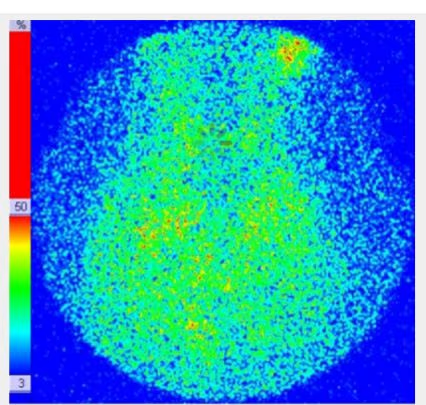
- Fig. 4: Hipercaptación (250 kcts en 359 seg) de distribución difusa en paciente con Enfermedad de Graves-Basedow.
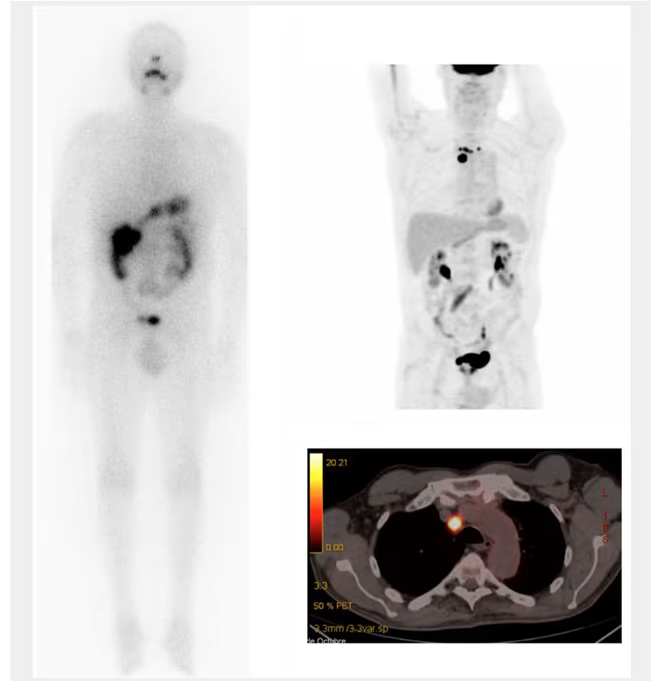
- Fig. 5: Nódulo hipercaptante autónomo que limita la visualización del resto de la glándula.
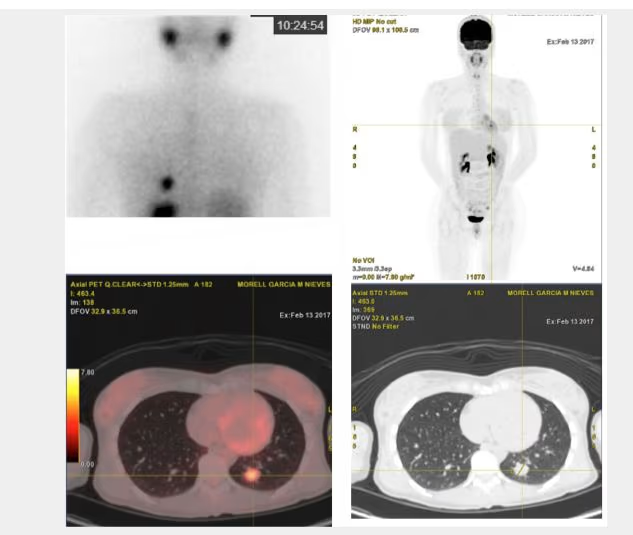
- Fig. 6: Nódulo sólido hipocaptante izquierdo en tiroides hipercaptante (250 kcts en 344 seg) en paciente con Enfermedad de Graves-Basedow.
- Fig. 7: Ausencia de captación tiroidea secundaria a tratamiento con amiodarona. Se ve solo actividad de fondo.
- Fig. 8: Tiroides sublingual.
6. INFORME AL CLÍNICO
- Datos del paciente y motivo de consulta.
- Captación tiroidea: aumentada / disminuida.
- Distribución de la actividad homogénea / nodular
- Si hay nódulos, hipo / hipercaptantes. Localización (lado y posición en el lóbulo). Conviene relacionarlos con la ecografía.
- Es interesante la información evolutiva con respecto a gammagrafías previas.
- Intentar contestar el motivo de la petición.